Vacinas - Covid-19
Atualmente existem quatro formas para uma vacina contra Covid-19 ser disponibilizada no país: registro, uso emergencial, importação excepcional ou pelo consórcio Covax Facility.
Os estudos clínicos de vacinas são conduzidos pelos laboratórios farmacêuticos e instituições de pesquisa. Como agência reguladora, o papel da Anvisa é definir a regulamentação do setor e avaliar os processos e dados recebidos, do ponto de vista de sua comprovação de qualidade, eficácia e segurança.
Acompanhe aqui os processos de aprovação de cada imunizante no país. Escolha a vacina abaixo para saber mais.
Quer notificar alguma reação adversa com a vacina? Clique aqui e saiba mais.
VACINAS APROVADAS
Autorização emergencial expirada
OUTRAS SITUAÇÕES
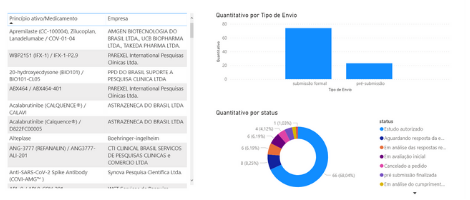
ESTUDOS CLÍNICOS
Notícias sobre as vacinas
Anvisa aprova atualização de vacina contra Covid-19
Vacina da empresa Zalika foi atualizada para a cepa XBB.1.5.
Anvisa aprova registro da vacina Spikevax monovalente
Novo imunizante protege contra a variante XBB 1.5 da Covid-19.
Anvisa autoriza ampliação dos prazos de validade das vacinas Comirnaty (Pfizer) monovalente e bivalente
Prazo de validade foi ampliado de 18 meses para 24 meses.
Nota da Anvisa: fake news sobre a vacina bivalente
A segurança e a eficácia da vacina foram comprovadas por meio de dados técnicos e científicos.